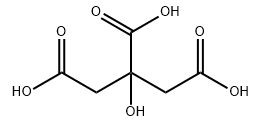
Acide citrique CAS n° 77-92-9
Numéro CAS :77-92-9
Formule chimiqueun: Expliquer la surface
Synonymes :
BETZ 6251
BETZ 0623
CULTURE VÉGÉTALE ANHYDRE SANS ACIDE CITRIQUE
MOQ (Quantité minimale de commande) :1 FCL (chargement complet d'un conteneur)
Apparence:Poudre blanche
Acide citrique CAS n° 77-92-9
L'acide citrique est un acide organique faible, blanc et cristallin, présent dans la plupart des plantes et chez de nombreux animaux, où il intervient dans la respiration cellulaire. Il contient trois groupes carboxyle, ce qui en fait un acide carboxylique, plus précisément tricarboxylique. Le nom « citron » provient du grec « kedromelon », signifiant pomme ou melon, en référence au fruit citron. Les textes grecs mentionnent « kitron », « kitrion » ou « kitreos » pour désigner le citron, un fruit oblong de plusieurs centimètres de long, issu du plant de citronnier (Citrus medica). Les citrons et les limes sont riches en acide citrique, qui peut représenter jusqu'à 8 % de leur poids sec.
| Propriétés chimiques de l'acide citrique |
| Point de fusion | 153-159 °C (litt.) |
| Point d'ébullition | 310 °C (décomposition) |
| densité apparente | 560 kg/m³ |
| densité | 1,67 g/cm3 à 20 °C |
| densité de vapeur | 7,26 (par rapport à l'air) |
| pression de vapeur | <0,1 hPa (20 °C) |
| indice de réfraction | 1 493 à 1 509 |
| FEMA | 2306 | ACIDE CITRIQUE |
| Fp | 100 °C |
| température de stockage | 2-8°C |
| solubilité | L'acide citrique se dissout également dans l'éthanol absolu (anhydre) (76 parties d'acide citrique pour 100 parties d'éthanol) à 15 °C. |
| formulaire | grincer |
| pka | 3,14 (à 20 °C) |
| couleur | Blanc |
| PH | 3,24 (solution à 1 mM) ; 2,62 (solution à 10 mM) ; 2,08 (solution à 100 mM) ; |
| Odeur | Inodore |
| Type d'odeur | inodore |
| source biologique | synthétique |
| limite d'explosivité | 8 %, 65 °F |
| Solubilité dans l'eau | soluble dans l'eau (1174g/L à 10°C, 1809g/L à 30°C, 3825g/L à 80°C). |
| Sensible | Hygroscopique |
| λmax | λ : 260 nm Amax : 0,20 λ : 280 nm Amax : 0,10 |
| Merck | 14.2326 |
| Numéro JECFA | 218 |
| BRN | 782061 |
| Stabilité: | Stable. Incompatible avec les bases, les agents oxydants puissants, les agents réducteurs et les nitrates métalliques. |
| Fonctions des ingrédients cosmétiques | CHÉLATION PARFUM TAMPON |
| InChIKey | كركنيبشكسنجكسهففيسن |
| LogP | -1.64 |
| Référence de la base de données CAS | 77-92-9 (Référence de la base de données CAS) |
| Référence de chimie du NIST | Acide 1,2,3-propanetricarboxylique, 2-hydroxy-(77-92-9) |
| Système d'enregistrement des substances de l'EPA | Acide citrique (77-92-9) |
| Informations de sécurité |
| Codes de danger | Xi,C,T |
| Déclarations de risques | 41-36/37/38-36/38-37/38-34-36-35-61-60 |
| Consignes de sécurité | 26-39-37/39-24/25-36/37/39-45-36-53 |
| lecteur | UN 1789 8/PG 3 |
| WGK Allemagne | 1 |
| RTECS | GE7350000 |
| F | 9 |
| TSCA | Répertorié TSCA |
| Code SH | 2918 14 00 |
| Données sur les substances dangereuses | 77-92-9 (Données sur les substances dangereuses) |
| Toxicité | DL50 chez la souris, le rat (mmol/kg) : 5,0, 4,6 i.p. (Gruber, Halbeisen) |
Application du produit acide citrique CAS n° 77-92-9
| L'acide citrique est un acide organique faible, un produit chimique de base, dont plus d'un million de tonnes sont produites chaque année par fermentation fongique à l'échelle industrielle à partir de solutions de sucre brut, comme la mélasse, et de souches d'Aspergillus niger. On le trouve en abondance dans les plantes, les tissus et les fluides animaux, ainsi que dans de nombreux fruits et légumes, notamment les agrumes comme le citron et le citron vert. L'acide citrique est principalement utilisé comme acidifiant, agent aromatisant et agent chélateur. Il était également employé comme agent de restriction chimique, en particulier dans les révélateurs du procédé au collodion et dans les solutions de nitrate d'argent utilisées pour sensibiliser les papiers salés et albuminés. |
Carbonate de strontium CAS n° 1633-05-2
Le carbonate de strontium (SrCO₃) (1633-05-2) est un sel de carbonate de strontium, présent à l'état naturel sous forme de strontianite. Il trouve des applications dans de nombreux secteurs industriels. Actuellement, les carbonates de strontium sont couramment utilisés comme colorant économique en pyrotechnie, car le strontium et ses sels produisent une flamme rouge pourpre. Le carbonate de strontium est généralement préféré aux autres sels de strontium dans les feux d'artifice en raison de son faible coût, de son caractère non hygroscopique et de sa capacité à neutraliser les acides. Il peut également servir à la fabrication de fusées de détresse routières, à la préparation de verres irisés, de peintures lumineuses, d'oxyde de strontium ou de sels de strontium, ainsi qu'au raffinage du sucre et de certains médicaments. Il est également recommandé comme substitut du baryum pour la production d'émaux mats. De plus, il est utilisé dans l'industrie céramique, où il entre dans la composition des émaux, et dans l'industrie électrique, où il sert à la production de ferrites de strontium pour la fabrication d'aimants permanents destinés aux haut-parleurs et aux aimants de porte. Le carbonate de strontium est également utilisé pour la fabrication de certains supraconducteurs tels que le BSCCO et aussi pour les matériaux électroluminescents.
| Propriétés chimiques du carbonate de strontium |
| Point de fusion | 1494 °C (litt.) |
| densité | 3,7 g/mL à 25 °C (litt.) |
| indice de réfraction | 1.518 |
| température de stockage | Atmosphère inerte, température ambiante |
| solubilité | acide aqueux dilué : légèrement soluble (litt.) |
| formulaire | Poudre |
| Gravité spécifique | 3.7 |
| couleur | blanc |
| PH | 7-8 (20°C, 0,01 g/L dans H2O) |
| Odeur | Inodore |
| Solubilité dans l'eau | Soluble dans le chlorure d'ammonium. Légèrement soluble dans l'ammoniaque et l'eau. |
| Merck | 14 8838 |
| Constante du produit de solubilité (Ksp) | pKsp : 9,25 |
| Stabilité: | Stable. Incompatible avec les acides forts. |
| InChIKey | Ledmerzjfzjbhffisal |
| LogP | -0.809 (est) |
| Référence de la base de données CAS | 1633-05-2 (Référence de la base de données CAS) |
| Système d'enregistrement des substances de l'EPA | Acide carbonique, sel de strontium (1:1) (1633-05-2) |
| Informations de sécurité |
| WGK Allemagne | - |
| TSCA | Répertorié TSCA |
| Code SH | 2836920000 |
| Données sur les substances dangereuses | 1633-05-2 (Données sur les substances dangereuses) |
Application du carbonate de strontium CAS n° 1633-05-2
Le composé SrCO3 est utilisé en pyrotechnie et dans la fabrication de ferrites céramiques. Il entre également dans la composition du verre irisé destiné aux tubes cathodiques des téléviseurs couleur. On l'utilise aussi dans le raffinage du sucre et la préparation d'autres sels de strontium. Son usage le plus courant est celui de colorant bon marché pour feux d'artifice. Le strontium et ses sels émettent une flamme rouge éclatante. Sa capacité à neutraliser l'acide est également très utile en pyrotechnie. Il est utilisé dans la fabrication de fusées de signalisation routières. Le carbonate de strontium est utilisé en électronique. Il sert à la fabrication des tubes cathodiques des téléviseurs couleur pour absorber les rayons X émis par le canon à rayons cathodiques. Le SrCO3 est utilisé dans la préparation du verre irisé, de l'oxyde de strontium ou des sels de strontium, ainsi que dans le raffinage du sucre. Il est largement utilisé dans l'industrie céramique comme ingrédient des émaux. Il agit comme fondant et modifie également la couleur de certains oxydes métalliques. Il est également utilisé dans la fabrication de ferrites de strontium pour les aimants permanents employés dans les haut-parleurs et les aimants de porte. Le carbonate de strontium permet de produire de nombreux composés de strontium différents par simple dissolution dans l'acide correspondant. Le bicarbonate de strontium n'a pas encore été isolé.
Salon des usines et des équipements
Délai de livraison rapide
Délai d'approvisionnement : 2 à 3 jours ouvrables. Délai de production : 7 à 10 jours ouvrables.